hPBMC在肿瘤免疫模拟中的yaboapp体育官网临床前应用进展
作者:
Sheri Barnes博士。
日期:
2020年7月
二月份,我们介绍了Covance利用人外周血单个核细胞开发的新型人源化小鼠平台的初步数据(hPBMC)植入.
我们的数据使用点头Cg-Prkdcscid Il2rgtm1Wjl公司/SzJ(NSG)小鼠鉴定出四种hPBMC供体,它们在hPBMC注射后至少有30天的治疗窗,持续的T细胞植入,以及两种人类异种移植模型MiaPaCa-2(胰腺)和A549(NSCLC)的生长,这两种移植模型在临床上表现出很强的稳定性hPBMC移植NSG小鼠.
我们现在提供了初步的疗效数据,证明在用pembrolizumab(Keytruda®,抗hPD-1)治疗后,使用带有MiaPaCa-2或A549人类异种移植物的hPBMC植入NSG小鼠。
实验设计
这些研究的目的是评价pembrolizumab在NSG小鼠中植入hPBMCs后对MiaPaCa-2或A549人类肿瘤模型的抗肿瘤反应。动物的护理和使用是按照AAALAC认可的实验动物护理和使用指南进行的。
NSG小鼠(Jackson Laboratories,Bar Harbor Maine,USA,品系#0005557)在肿瘤形成后(约105-118mm)静脉注射来自三种不同正常健康供体(Hemacare,Los Angeles CA,USA)的HPBMC三). 注射hPBMC后第二天开始用pembrolizumab治疗。对pembrolizumab的反应,确定移植物抗宿主病(GvHD)样特征的评估,并在两个时间点采集全血用于流式细胞术分析人类淋巴细胞标记物,以确认供体植入CD45+细胞,包括CD4+和CD8+T细胞。
MiaPaCa-2和A549对hPBMC移植小鼠肿瘤生长的影响
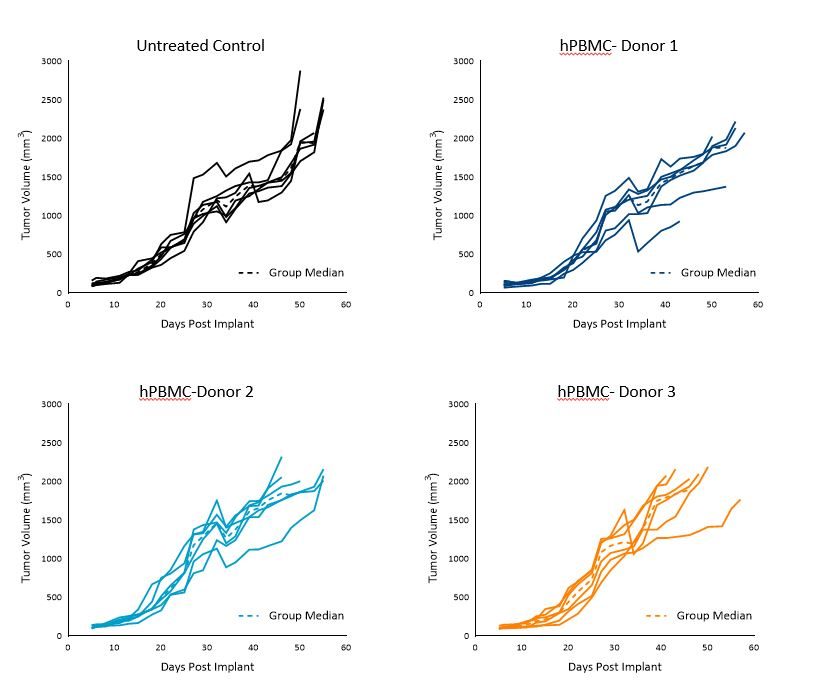
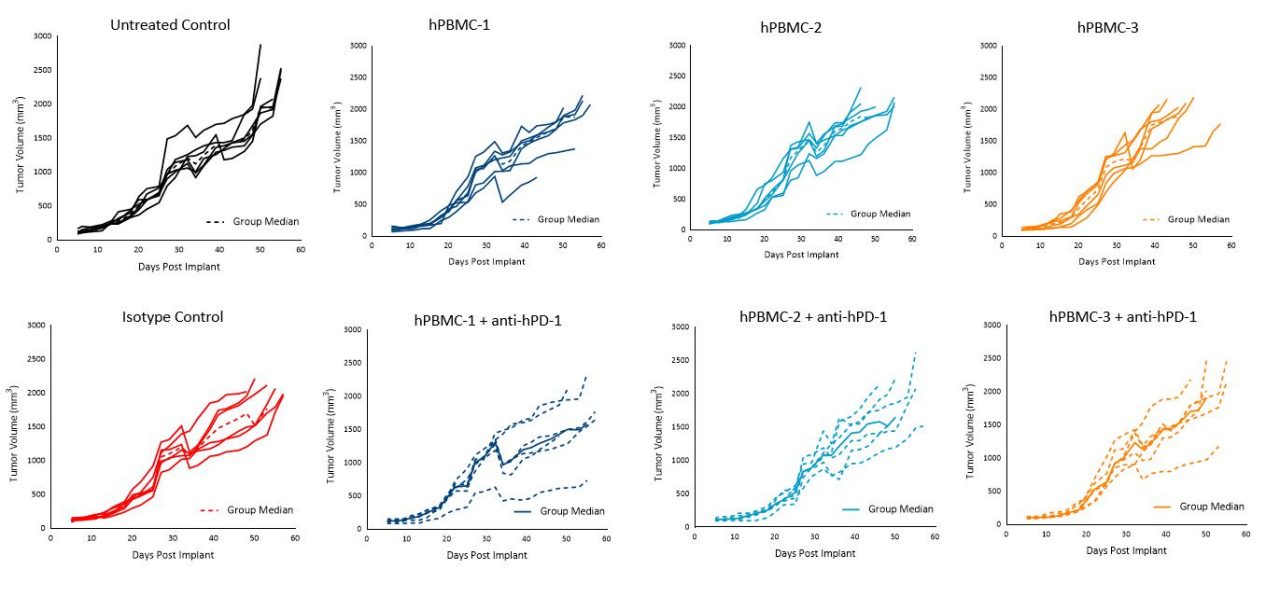
未治疗对照组动物的MiaPaCa-2肿瘤倍增时间(Td)为~7天,各供者组给予hPBMCs的动物的Td为~5~7天。
肿瘤生长均匀,平均肿瘤体积为1000~1200mm三然而,到了第36天,所有三个供体在第36天之后都出现了一些组内和组间的变异。1000mm前肿瘤生长三似乎没有受到HPBMC植入的影响(图1)。
这些结果表明,使用这三种供体中的任何一种都适用于评估时间为1000mm的MiaPaCa-2疗效研究三.
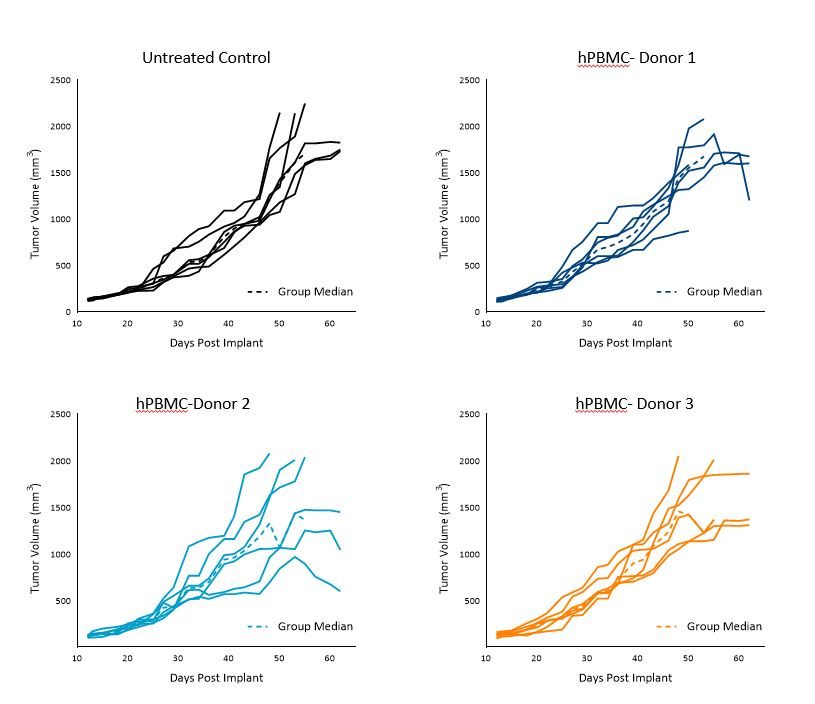
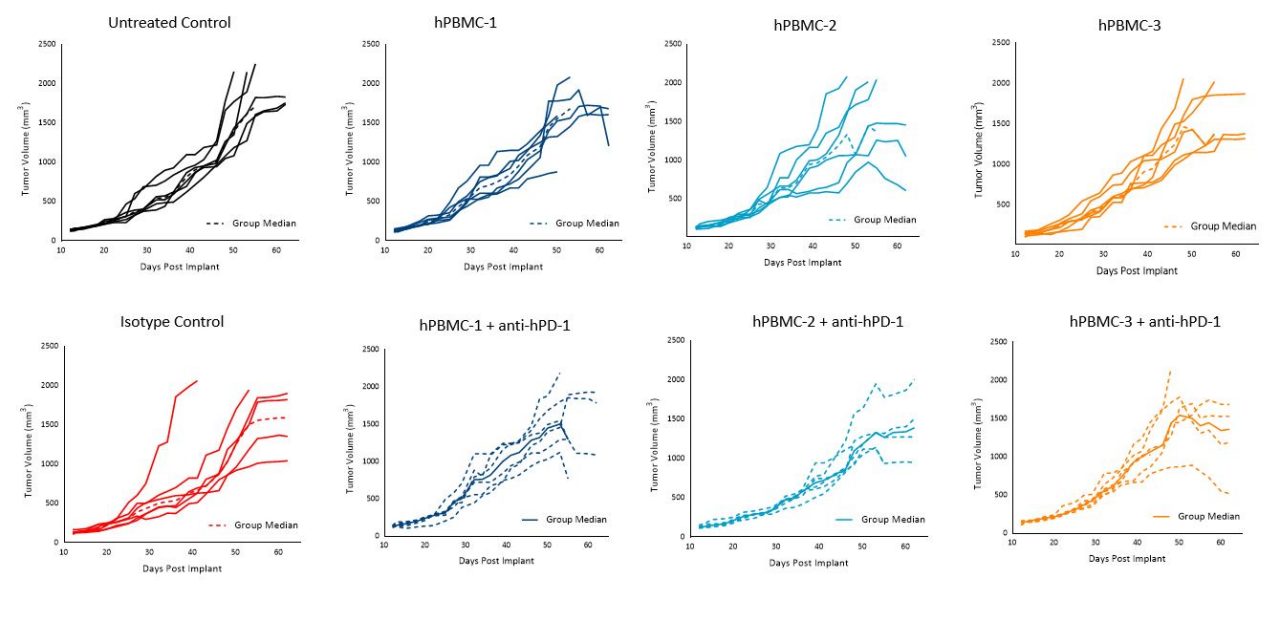
未治疗对照组动物的a549td为~11天,各供者组给予hPBMCs的动物的Td为9~12天。
肿瘤与供者1和供者3的hPBMCs均匀生长,平均肿瘤体积为1000-1200mm三到第40天,在第40天以后,生长会有一些变化。
组内变异性在携带A549肿瘤和来自供体2的HPBMC的小鼠中最为明显(图2)。
这些结果表明,捐赠者1和捐赠者3是最适合的A549型使用1000mm TES进行疗效研究三.
人淋巴细胞的植入和持续性
通过对研究小鼠外周血中人类免疫细胞标记物的免疫表型分析,在给予hPBMC后第28天和第38天(MiaPaCa-2)或第42天(A549)评估植入情况。
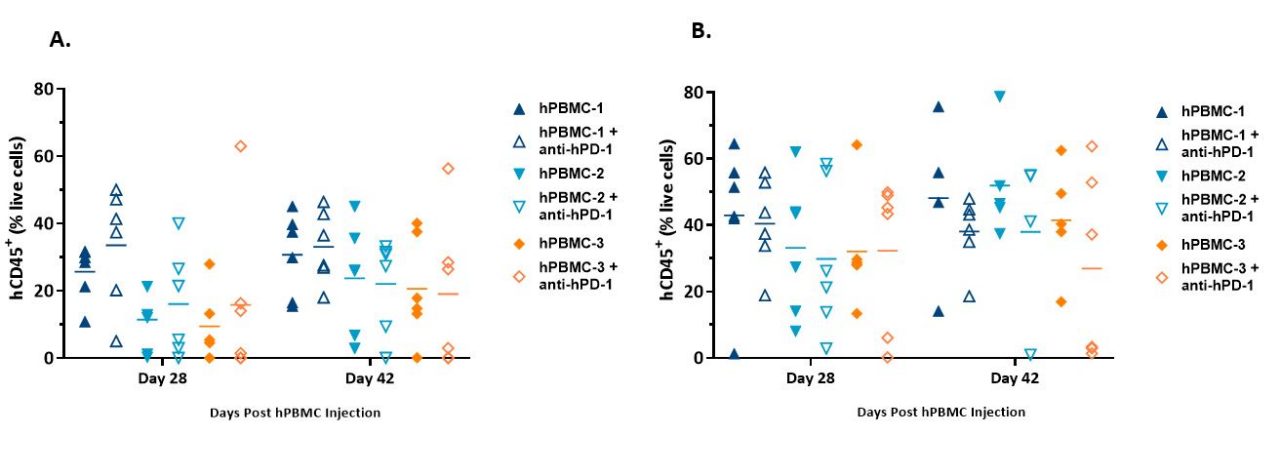
流式细胞术标记包括mCD45、hCD45、hCD3、hCD4和hCD8。人CD45+细胞占来自携带MiaPaCa-2(图3A)或A549肿瘤(图3B)动物的活细胞的百分比如下所示,并用作hPBMC植入的指标。
我们发现在两个时间点在所有献血者的全血中检测到hCD45+细胞,这与已发表的文献一致。1
虽然组内变异明显,但在第一个和第二个时间点之间植入的平均程度保持一致或增加。结果表明,hPBMC植入A549肿瘤动物体内的比例略高于植入MiaPaCa-2肿瘤动物体内的比例,这与我们最初的模型建立数据一致。
目前,尚不清楚这是否是研究变异性的正常研究的结果,或者是否存在植入的模型依赖性。
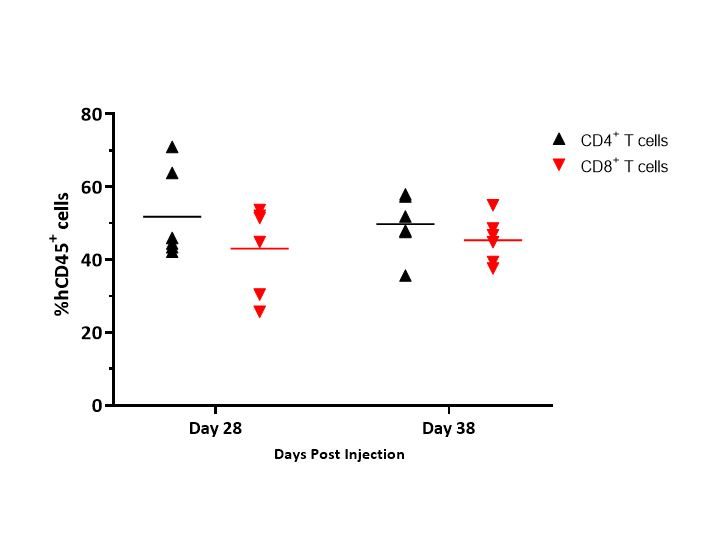
图4举例说明了全血中CD4+和CD8+T细胞的分布,并说明了T细胞在不同时间点的分布是一致的。
虽然这些数据仅代表了MiaPaCa-2肿瘤小鼠的供体1,但在供体和受试模型中报告了类似的数据。
具体而言,在MiaPaCa-2荷瘤小鼠中,CD4+和CD8+T细胞的分布范围分别为42-65%和32-46%,在A549荷瘤小鼠中,CD4+和CD8+T细胞的分布范围分别为51-67%和22-44%(数据未显示)。
GvHD症状的发生是通过体重和临床观察来监测的;虽然在这些研究中没有病理学证实,但在这些模型中观察到的症状与疾病密切相关2和以前的数据(数据未显示)。
对Pembrolizumab的反应
有趣的是,pembrolizumab治疗hPBMC移植小鼠,在试验条件下对任何供体的MiaPaCa-2或A549肿瘤生长没有影响(图5和图6)。
在这篇文章中,关于pembrolizumab在荷MiaPaCa-2肿瘤的hPBMC移植人源化小鼠体内的反应的文献很少。
尽管如此,我们的数据还是反映了大量关于胰腺肿瘤对免疫肿瘤药物的难治性的文献。三如前所述,pembrolizumab对A549的反应似乎是温和的,而且这种反应似乎是供体依赖性的。4
尽管pembrolizumab对A549或MiaPaCa-2始终缺乏应答,但这些模型对于使用抗hPD-1的合理组合策略的治疗方法是有用的,因为不同供体的不同应答存在显著的改善和评估空间。
向NSG小鼠施用hPBMCs可导致人类T细胞在小鼠体内持续存在,而对MiaPaCa-2或A549肿瘤生长的影响最小。这种方法代表了一个强大的临床前平台,以检查新的人类药物的影响,利用人类Tyaboapp体育官网淋巴细胞直接抗肿瘤活性具有直接的临床意义。
未来的工作将通过流式细胞术证明人T细胞在肿瘤和周围的浸润,并用FDA批准的免疫疗法治疗用hPBMCs重组的NSG小鼠的人肿瘤异种移植物。
Covance已经储存了这些人类PBMC捐赠者,以满足您的研究需要。拜托联系我们的临床前肿瘤科学yaboapp体育官网家看看hPBMC移植的NSG小鼠如何用于下一步的翻译研究免疫肿瘤学研究.
参考文献:
1托德·皮尔森、戴尔·L·格雷纳和伦纳德·D·舒尔茨。建立“人源化”小鼠研究人体免疫功能。2008第15章:第15.21单元
2Sina Naserian、Mathieu Leclerc、Allan Thiolat、Caroline Pilon、Cindy Le Bret、Yazid Belkacemi、Sébastien Maury、Frédéric Charlotte和JoséL.Cohen。急性移植物抗宿主病小鼠模型的简单、可重复和有效的临床分级系统。2018前面。在Immun。(9): 10.
三。罗伯特J.托菲、朱宇文和理查德D.舒利克。胰腺癌免疫治疗:障碍与突破。2018安胃肠外科。2(4): 274–281.
4林寿恒、黄国华、程林林、李臻、肖义仁、邓秋华、姜玉川、李百恒、林思淼、王苏娜、吴启亭、姚慧慧、曹苏、杨莉、刘彭涛、魏伟、裴端青、姚瑶、温哲生、张旭超、吴义龙、张振峰、崔树忠、孙晓芳、钱学明、李鹏。建立外周血单个核细胞来源的人源性肺癌小鼠模型,研究PD-L1/PD-1靶向免疫治疗的疗效。2018单克隆抗体。10(8): 1301–1311.