伴随诊断
诊断与治疗是具有挑战性的一个新伴侣的并行发展 - 但有针对性的测试或生物标记证明你的治疗的疗效的价值从未如此巨大。精密医学需要患者分层 - 确定谁更有可能从治疗中获益的患者的目标;伴随诊断也能缩短开发时间和Rx开发成本,可能会导致更有利的报销,可以说明比较效益。
一个新的选项 - 所谓的互补诊断 - 提供有关药物是如何使用的其他信息,但是从伴随诊断不同。我们支持前两种FDA批准的互补诊断的发展,可以帮助你衡量你的战略选择。
了解我们如何投资未来的精准医疗
你的治疗和诊断的 - 完美和谐。
科万斯是独特的装备,以支持您的个性化药物的发展与证明的途径,以成功。
选择与您的途径体外诊断(IVD)或实验室开发的测试(LDT)
获取从开发到验证的各种生物标志物专业知识
收到通知的监管指导,市场准入战略沿
广度和深度的平衡。具有治疗领域和平台的相关经验
无情的一致性。全球统一临床试验的结果
独特的见解。知情的监管指导和支持
商业化的解决方案。一个合作伙伴,可以帮助你制定和实施你的CDx市场准入战略和启动
广度和深度的平衡。具有治疗领域和平台的相关经验
无情的一致性。全球统一临床试验的结果
独特的见解。知情的监管指导和支持
商业化的解决方案。一个合作伙伴,可以帮助你制定和实施你的CDx市场准入战略和启动
Covance和LabCorp共同拥有成功开发和商业化CDx的工具和跟踪记录。
你的治疗需要一个伴侣;你需要一个足智多谋的合作伙伴。
伴生诊断(CDx)可以将个性化医疗的承诺变成现实。在我们团队的医疗和科学主题专家横跨所有治疗领域的支持下,你将协调你的Rx和Dx的发展目标。随着您的治疗方案获得批准,我们将帮助您的CDx更快地进入市场。
选择权:在体外试验或实验室开发的测试。
CDx商业化的最佳途径可能不涉及传统的分布式体外诊断工具)。涉及孤儿药、压缩时间线或操作复杂性的项目可能会因fda批准的基于实验室的检测而兴旺发达。您将最大限度地减少前期投资,并减轻与广泛分布的IVD工具包相关的潜在风险。作为您的合作伙伴,我们将开发和验证您的测试,领导提交监管文件,并为您的测试提供立即的全球准入,使您的测试快速进入市场。
无论是追求一个实验室开发的测试(LDT)或IVD,你需要专家的指导,团结你的CDx将和治疗的发展和提取的试验中最值。拥有超过25年的临床试验经验和80+诊断传递给市场,我们具备雄厚的技术库,战略的灵活性和科学的见解,可以帮助您确定商业化的最佳途径。
全球范围和一致性——驱动你的伴侣诊断验证。
CDx开发的靶向性要求在一系列患者人群中设计和验证检测方法。您可以利用我们的全球覆盖,分销网络和标准化效率在我们的协调中心实验室。而且,有了世界各地的高水平的调查网站,你每次都能得到高质量的、组合的数据。
您的可能性。我们诊断的解决方案。
以上的相关能力的清单,我们CDx将服务协同工作,支持并加速您共同开拓力度的各个方面。有什么可以代替经验:我们支持〜25 FDA认证或批准的同伴19诊断设备 - 包括那些HER-2,KRAS,EGFR,BRAF和ALK。与单一的战略合作伙伴统一的CDx将追求,其中包括:
- 生物标志物的识别和发展
- 分析可行性,概念论证和验证
- 全球临床试验试验
- 设备制造和商业化伙伴关系
- 上市前批准(PMA)的应用开发和提交
- 市场准入策略、启动支持和商业化指导
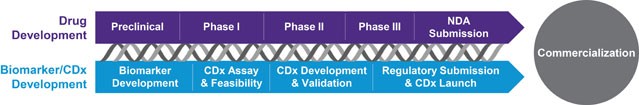
凭借在肿瘤学、免疫肿瘤学、中枢神经系统、传染病和炎症等领域的伴随诊断和补充诊断方面的经验,我们可以提供科学娴熟、专注的专业知识,推动您CDx的成功。

